UP Board Solutions for Class 10 Science Chapter 2 Acids, Bases and Salts
UP Board Solutions for Class 10 Science Chapter 2 Acids, Bases and Salts (अम्ल, क्षार एवं लवण)
पाठगत हल प्रश्न
[NCERT IN-TEXT QUESTIONS SOLVED]
खंड-2.1 ( पृष्ठ संख्या 20)
प्रश्न 1.
आपको तीन परखनलियाँ दी गई हैं। उनमें से एक में आसवित जल एवं शेष दो में से एक में अम्लीय विलयन तथा दूसरे में क्षारीय विलयन है। यदि आपको केवल लाल लिटमस पत्र दिया जाता है, तो आप प्रत्येक परखनली में रखे गए पदार्थों की पहचान कैसे करेंगे?
उत्तर
सबसे पहले दिए गए लाल लिटमस पत्र को बारी-बारी से तीनों परखनलियों में डालते हैं। हम पाते हैं कि किसी एक परखनली में यह लिटमस पत्र नीला हो गया। चूँकि क्षारीय विलयन में लाल लिटमस पत्र नीला हो जाता है। अतः इस परखनली में अवश्य ही क्षारीय विलयन है। अब शेष दो परखनलियों में इस नीले लिटमस पत्र को डालते हैं। इसमें दो स्थितियाँ हो सकती हैं
- लिटमस पत्र पुनः लाल हो जाएगा।
- लिटमस पत्र नीला ही रह जाएगा।
जिस परखनली में लिटमस पत्र लाल हो गया उसमें अम्लीय विलयन तथा जिसमें रंग अपरिवर्तित अर्थात् नीला ही रहा उसमें आसवित जल होगा।
खंड 2.2 (पृष्ठ संख्या 24)
प्रश्न 1.
पीतल एवं ताँबे के बर्तनों में दही एवं खट्टे पदार्थ क्यों नहीं, रखने चाहिए?
उत्तर
पीतल (Cu तथा Zn का मिश्रधातु) तथा ताँबे के बर्तनों में दही एवं खट्टे पदार्थ इसलिए नहीं रखे जाते हैं, क्योंकि इसमें अम्ल मौजूद होते हैं, जो इससे अभिक्रिया करके हानिकारक (विषैले) यौगिक (toxic compounds) बनाते हैं। जिसके कारणवश ये खाने लायक नहीं रह जाते। अम्ल की अभिक्रिया से धातु के बर्तन भी संक्षारित हो जाते हैं।
प्रश्न 2.
धातु के साथ अम्ल की अभिक्रिया होने पर सामान्यतः कौन-सी गैस निकलती है? एक उदाहरण के द्वारा समझाइए। इस गैस की उपस्थिति की जाँच आप कैसे करेंगे?
उत्तर
धातु के साथ अम्ल की अभिक्रिया से सामान्यतः हाइड्रोजन गैस निकलती है। उदाहरण-
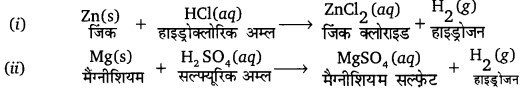
जाँच-जलती हुई माचिस की तीली परखनली के मुँह के पास ले जाने पर फट-फट की आवाज़ (Pop sound) के साथ जलने लगती है जो यह दर्शाता है कि H2 गैस बनी है।
प्रश्न 3.
कोई धातु यौगिक A तनु हाइड्रोक्लोरिक अम्ल के साथ अभिक्रिया करती है तो बुदबुदाहट उत्पन्न होती है। इससे उत्पन्न | गैस जलती मोमबत्ती को बुझा देती है। यदि उत्पन्न यौगिकों में से एक कैल्सियम क्लोराइड है, तो इस अभिक्रिया के लिए संतुलित रासायनिक समीकरण लिखिए।
उत्तर
धातु के यौगिक A CaCO3 (कैल्शियम कार्बोनेट) है।
![]()
खंड 2.3 ( पृष्ठ संख्या 27)
प्रश्न 1.
HCI, HNO आदि जलीय विलयन में अम्लीय अभिलक्षण क्यों प्रदर्शित करते हैं, जबकि ऐल्कोहॉल एवं ग्लूकोज़ जैसे यौगिकों के विलयनों में अम्लीयता के अभिलक्षण नहीं प्रदर्शित होते हैं।
उत्तर
HCl, HNO3 आदि के जलीय विलयन में H+ आयन बनता है, जिसके कारण ये अम्लीय अभिलक्षण प्रदर्शित करते हैं जबकि ऐल्कोहॉल एवं ग्लूकोज़ जैसे यौगिकों के जलीय विलयनों में H+ आयन नहीं बनता है। इसलिए ये अम्लीयता के अभिलक्षण नहीं प्रदर्शित करते हैं।
प्रश्न 2.
अम्ल का जलीय विलयन क्यों विद्युत का चालन करता है?
उत्तर
अम्ल का जलीय विलयन H+ आयन उत्पन्न करता है जिसके कारण विद्युत धारा का प्रवाह (चालन) होता है।
प्रश्न 3.
शुष्क हाइड्रोक्लोरिक गैस शुष्क लिटमस पत्र के रंग को क्यों नहीं बदलती है?
उत्तर
शुष्क हाइड्रोक्लोरिक गैस शुष्क लिटमस पत्र के रंग को इसलिए नहीं बदल पाती है, क्योंकि जल की अनुपस्थिति में HCl से H+ आयन अलग नहीं हो पाता है। अर्थात् सिर्फ जलीय माध्यम में ही H+ आयन बनता है।
प्रश्न 4.
अम्ल को तनुकृत करते समय यह क्यों अनुशंसित करते हैं कि अम्ल को जल में मिलाना चाहिए, न कि जल को अम्ल में?
उत्तर
क्योंकि जल में अम्ल या क्षारक के घुलने की प्रक्रिया अत्यंत ऊष्माक्षेपी होती है। जल में सांद्र नाइट्रिक अम्ल या सल्फ्यूरिक अम्ल को मिलाते समय अत्यंत सावधानी रखनी चाहिए। अम्ल को सदैव धीरे-धीरे तथा जल को लगातार हिलाते हुए जल में मिलाना चाहिए। सांद्र अम्ल में जल मिलाने पर उत्पन्न हुई ऊष्मा के कारण मिश्रण आस्फलित होकर बाहर आ सकता है तथा आप जल सकते हैं। साथ ही अत्यधिक स्थानीय ताप के कारण प्रयोग में उपयोग किया जा रहा काँच का पात्र भी टूट सकता है।
प्रश्न 5.
अम्ल के विलयन को तनुकृत करते समय हाइड्रोनियम आयन (H3O+) की सांद्रता कैसे प्रभावित हो जाती है?
उत्तर
अम्ल के विलयन में जल मिलाने पर H+ आयन H20 से संयोग कर (H3O+) आयन बनाते हैं। अम्ल के विलयन को तनुकृत करने पर हाइड्रोनियम आयन (H3O+) की सांद्रता में कमी हो जाती है।
प्रश्न 6.
जब सोडियम हाइड्रॉक्साइड विलयन में आधिक्य क्षारक मिलाते हैं, तो हाइड्रॉक्साइड (OH+) की सांद्रता कैसे प्रभावित होती है?
उत्तर
जब सोडियम हाइड्रॉक्साइड (NaOH) के विलयन में आधिक्य क्षारक मिलाते हैं तो (OH–) आयन की सांद्रता बढ़ जाती है।
खंडे 2.4 ( पृष्ठ संख्या 31)
प्रश्न 1.
आपके पास विलयन ‘A’ एवं ‘B’ है। विलयन ‘A’ के pH का मान 6 है एवं विलयन ‘B’ के PH का मान 8 है। किस विलयन में हाइड्रोजन आयन की सांद्रता अधिक है? इनमें से कौन, अम्लीय है तथा कौन-सा क्षारकीय?
उत्तर
विलयन ‘A’ का PH = 6 है, इसलिए यह अम्लीय होगा, क्योंकि pH <7 है। विलयन ‘B’ का PH = 9 है इसलिए यह क्षारकीय होगा, क्योंकि pH > 7 है। विलयन ‘A’ में H+ आयन की सांद्रता अधिक है।
प्रश्न 2.
H’ (aq) आयन की सांद्रता का विलयन की प्रकृति पर क्या प्रभाव पड़ता है?
उत्तर
जैसे-जैस हाइड्रोजन आयन H+ (aq) आयन की सांद्रता बढ़ती है, विलयन और अधिक अम्लीय होता जाता है।
प्रश्न 3.
क्या क्षारकीय विलयन में H+ (aq) आयन होते हैं? अगर हाँ, तो यह क्षारकीय क्यों होते हैं?
उत्तर
हाँ, H+ (aq) आयन क्षारकीय विलयन में भी होते हैं परंतु इसकी सांद्रता (OH) आयनों की सांद्रता से कम होती है, जिसके कारणवश यह विलयन क्षारकीय होते हैं।
प्रश्न 4.
कोई किसान खेत की मृदा की किस परिस्थिति में बिना बुझी हुआ चूना (कैल्शियम ऑक्साइड), बुझा हुआ चूना (कैल्शियम हाइड्रॉक्साइड) या चॉक (कैल्शियम कार्बोनेट) का उपयोग करेगा?
उत्तर
जब खेत की मृदा अम्लीय होती है तभी किसान इसमें कैल्शियम ऑक्साइड (CaO), कैल्शियम हाइड्रॉक्साइड [Ca(OH)2] तथा कैल्शियम कार्बोनेट (CaCO3) मिलाते हैं ताकि मिट्टी उदासीन हो जाए या इसका pH परास खेती के लिए उपयुक्त हो जाए।
खंड 2.5 ( पृष्ठ संख्या 36)
प्रश्न 1.
CaOCl2 यौगिक का प्रचलित नाम क्या है?
उत्तर
CaOCl2 यौगिक का प्रचलित नाम विरंजक चूर्ण है।
प्रश्न 2.
उस पदार्थ का नाम बताइए जो क्लोरीन से क्रिया करके विरंजक चूर्ण बनाता है।
उत्तर
शुष्क बुझा हुआ चूना (कैल्शियम हाइड्रोक्सॉइड–Ca(OH)2) क्लोरीन से अभिक्रिया करके विरंजक चूर्ण बनाता है।
Ca(OH)2 + Cl2 → CaOCl2 + H2O
प्रश्न 3.
कठोर जल को मृदु करने के लिए किस सोडियम यौगिक का उपयोग किया जाता है?
उत्तर
सोडियम कार्बोनेट (Na2CO) इसे धोने का सोडा भी कहा जाता है।
प्रश्न 4.
सोडियम हाइड्रोजन कार्बोनेट के विलयन को गर्म करने पर क्या होगा? इस अभिक्रिया के लिए समीकरण लिखिए।
उत्तर
जब सोडियम हाइड्रोजन कार्बोनेट के विलयन को गर्म किया जाता है तो यह अपघटित होकर सोडिधम कार्बोनेट, जल एवं CO2 गैस का निर्माण करता है। अभिक्रिया इस प्रकार होती है-
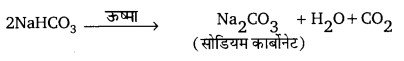
प्रश्न 5.
प्लास्टर ऑफ पेरिस की जल के साथ अभिक्रिया के लिए समीकरण लिखिए।
उत्तर
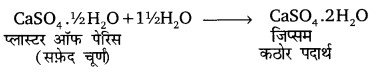
पाठ्यपुस्तक से हल प्रश्न
[NCERT TEXTBOOK QUESTIONS SOLVED]
प्रश्न 1.
कोई विलयन लाल लिटमस को नीला कर देता है, इसका pH संभवतः क्या होगा?
(a) 1
(b) 4
(c) 5
(d) 10
उत्तर
(d) 10 (संकेत-क्योंकि क्षारीय विलयन में लाल लिटमस नीला हो जाता है जिसका pH>7 होता है।)
प्रश्न 2.
कोई विलयन अंडे के पिसे हुए कवच से अभिक्रिया कर एक गैस उत्पन्न करता है जो चूने के पानी को दुधिया कर देती है। इस विलयन में क्या होगा?
(a) NaCl
(b) HCl
(C) LICl
(d) KCl
उत्तर
(b) HCl (संकेत–क्योंकि अंडे के कवच में CaCO3 होता है, जो HCl अम्ल से अभिक्रिया कर CO2 गैस बनाता है। CO2 गैस चूने के पानी को दुधिया कर देती है।
प्रश्न 3.
NaOH का 10 ml विलयन HCl के 8 ml विलयन से पूर्णत: उदासीन हो जाता है। यदि हम NaOH के उसी विलयन का 20 ml लें तो इसे उदासीन करने के लिए HCl के उसी विलयन की कितनी मात्रा की आवश्यकता होगी?
(a) 4 mL
(b) 8 mL
(C) 12 mL
(d) 16 mL
उत्तर
(d) 16 mL
प्रश्न 4.
अपच का उपचार करने के लिए निम्न में से किस औषधि का उपयोग होता है?
(a) एंटीबायोटिक (प्रतिजैविक)
(b) ऐनालजेसिक (पीड़ाहारी)
(C) ऐन्टैसिड
(d) एंटीसेप्टिक (प्रतिरोधी)
उत्तर
(C) ऐन्टैसिड
प्रश्न 5.
निम्न अभिक्रिया के पहले शब्द-समीकरण लिखिए तथा उसके बाद संतुलित समीकरण लिखिए
(a) तनु सल्फ्यूरिक अम्ल दानेदार जिंक के साथ अभिक्रिया करता है।
(b) तनु हाइड्रोक्लोरिक अम्ल मैग्नीशियम पट्टी के साथ अभिक्रिया करता है।
(C) तनु सल्फ्यूरिक अम्ल ऐलुमिनियम चूर्ण के साथ अभिक्रिया करता है।
(d) तनु हाइड्रोक्लोरिक अम्ल लौह के रेतन के साथ अभिक्रिया करता है।
उत्तर

प्रश्न 6.
ऐल्कोहॉल एवं ग्लूकोज जैसे यौगिकों में भी हाइड्रोजन होते हैं, लेकिन इनका वर्गीकरण अम्ल•की तरह नहीं होता | है। एक क्रियाकलाप द्वारा इसे सिद्ध कीजिए।
उत्तर
विधि-
- ग्लूकोज, ऐल्कोहॉल तथा हाइड्रोक्लोरिक अम्ल का विलयन लीजिए।
- एक कॉर्क पर दो कीलें लगाकर कार्क को 100 ml के बीकर में रख दीजिए।
- चित्र 2.6 के अनुसार कीलों को 6 वोल्ट की एक बैट्री के दोनों टर्मिनलों के साथ एक बल्ब तथा स्विच के माध्यम से जोड़ दीजिए। अब बीकर में थोड़ा तनु HCl डालकर विद्युत धारा प्रवाहित कीजिए।
- अब स्विच ऑन कीजिए आप देखेंगे कि बल्ब जल उठता है।
- इस क्रियाकलाप को HCl के स्थान पर बारी-बारी से ग्लूकोज और ऐल्कोहॉल के विलयन के साथ करिए।
अवलोकन- आप पाएँगे कि ऐल्कोहॉल और ग्लूकोज़ की स्थिति में बल्ब नहीं जलता है, क्योंकि विलयनों में H+ आयन नहीं बनता है।
निष्कर्ष- ग्लूकोज़ और ऐल्कोहॉल H+ आयन नहीं उत्पन्न करते हैं। किसी विलयन में विद्युत धारा का प्रवाह आयनों द्वारा होता है। इसलिए इन्हें अम्ल नहीं कहा जाता है।
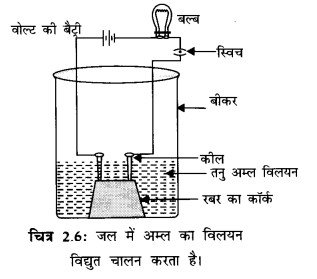
प्रश्न 7.
आसवित जल विद्युत का चालक क्यों नहीं होता, जबकि वर्षा । जल होता है?
उत्तर
- आसवित जल शुद्ध होते हैं, जिसमें आयन नहीं बनता है तथा विद्युत चालन करता है। विद्युत का चालन आयनों द्वारा होता है।
- वर्षा के जल में थोड़ी मात्रा में अम्ल होते हैं, क्योंकि वायु में उपस्थित SO2और NO2 गैस जल में मिलकर इसे अम्लीय बना देते हैं। ये अम्ल (H+) आयन उत्पन्न करते हैं, जिसके कारण विद्युत धारा का चालन हो जाता है।
प्रश्न 8.
जल की अनुपस्थिति में अम्ल का व्यवहार अम्लीय क्यों नहीं होता है?
उत्तर
क्योंकि जल की अनुपस्थिति में अम्लों से H+ आयन पृथक नहीं हो पाते हैं, इसलिए अम्ल का व्यवहार अम्लीय नहीं होता है। केवल जल की उपस्थिति में ही H+ आयन अलग हो पाते हैं तथा अम्लीय अभिलक्षण दर्शाने के लिए आयनों का बनना जरूरी होता है।
प्रश्न 9.
पाँच विलयनों A, B, C, D, व E की जब सार्वत्रिक सूचक से जाँच की जाती है, तो pH के मान क्रमशः 4, 1, | 11, 7 एवं 9 प्राप्त होते हैं। कौन-सा विलयन
(a) उदासीन है?
(b) प्रबल क्षारीय है?
(C) प्रबल अम्लीय है?
(d) दुर्बल अम्लीय है?
(e) दुर्बल क्षारीय है?
pH के मानों को हाइड्रोजन आयन की सांद्रता के आरोही क्रम में व्यवस्थित कीजिए।
उत्तर
विलयन pH के मान

प्रश्न 10.
परखनली ‘A’ एवं ‘B’ में समान लंबाई की मैग्नीशियम की पट्टी लीजिए। परखनली ‘A’ में हाइड्रोक्लोरिक अम्ल (HCl) तथा परखनली ‘B’ में ऐसिटिक अम्ल (CH3COOH) डालिए। दोनों अम्लों की मात्रा तथा सांद्रता समान हैं। किस परखनली में अधिक तेज़ी से बुदबुदाहट होगी तथा क्यों?
उत्तर
परखनली A में बुदबुदाहट अधिक तेजी से होती है, क्योंकि HCl एक प्रबल अम्ल है, जो पूर्णतः वियोजित होकर H+ और Cl– आयन अधिक मात्रा में बनाते हैं जबकि CH3COOH एक दुर्बल अम्ल है, जो कम मात्रा में H’ आयन बनाते हैं क्योंकि यह कम विघटित हो पाता है।
प्रश्न 11.
ताजे दूध के pH का मान 6 होता है। दही बन जाने पर इसके pH के मान में क्या परिवर्तन होगा? अपना
उत्तर
समझाइए। उत्तर दूध से दही बनने की प्रक्रिया में लैक्टिक अम्ल का निर्माण होता है, जिसके कारण इसका pH: 6 से कम हो जाता है।
प्रश्न 12.
एक ग्वाला ताजे दूध में थोड़ा बेकिंग सोडा मिलाता है।
(a) ताज़ा दूध के pH के माना को 6 से बदलकर थोड़ा क्षारीय क्यों बना देता है?
(b) इस दूध को दही बनने में अधिक समय क्यों लगता है?
उत्तर
- ताज़ा दूध के pH के मान को 6 से बदलकर थोड़ा क्षारीय इसलिए किया जाता है, क्योंकि क्षारीय दूध अधिक समय तक खराब नहीं होता है।
- इस दूध को दही बनने में अधिक समय इसलिए लगता है, क्योंकि इस प्रक्रिया में बना लैक्टिक अम्ल पहले क्षारक को उदासीन करता है फिर अम्लीय होता है, जिसके कारण दही बनता है।
प्रश्न 13.
प्लास्टर ऑफ पेरिस को आर्द्र-रोधी बर्तन में क्यों रखा जाना चाहिए? इसकी व्याख्या कीजिए।
उत्तर
प्लास्टर ऑफ पेरिस को आर्द्र-रोधी (moisture-proof) बर्तनों में इसलिए रखा जाता है, क्योंकि यह आर्द्रता की उपस्थिति में जल को अवशोषित कर ठोस पदार्थ जिप्सम बनाती है, जिसके कारण इसमें जल के साथ मिलकर जमने का गुण नष्ट हो जाता है।
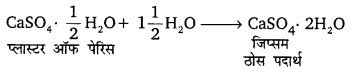
प्रश्न 14.
उदासीनीकरण अभिक्रिया क्या है? दो उदाहरण दीजिए।
उत्तर
अम्ल और क्षारक की अभिक्रिया से लवण एवं जल बनते हैं, जिसे उदासीनीकरण अभिक्रिया कहते हैं। चूँकि सभी
अम्ल H+(aq) तथा सभी क्षारक OH–(aq) बनाते हैं।

प्रश्न 15.
धोने का सोडा एवं बेकिंग सोडा के दो-दो प्रमुख उपयोग बताइए।
उत्तर
1. धोने के सोडे का उपयोग-
- सोडियम कार्बोनेट (धोने का सोडा) का उपयोग काँच, साबुन एवं कागज उद्योगों में होता है।
- सोडियम कार्बोनेट का उपयोग घरों में साफ़-सफ़ाई के लिए होता है।
2. बेकिंग सोडा (NaHCO3) का उपयोग-
- बेकिंग पाउडर बनाने में जो बेकिंग सोडा और टार्टरिक अम्ल का मिश्रण है।
- इसका उपयोग सोडा-अम्ल अग्निशामक में भी किया जाता है।